|
Chapitre IV : Les lasers ***** |
table des matières de
la page :
3.
Caractéristiques des lasers :
d) Les microscopes opératoires :
II- Les lasers et le milieu médical :
1. Les effets
biologiques du laser :
2. Action du
laser sur un milieu :
3. Exemples d’utilisation des
lasers :
______________________________________________________________________

I- Introduction
Le terme laser provient des initiales des mots anglais “
Light Amplification by Stimulated Emission of Radiations » qui signifie en
Français “ Amplification lumineuse par émission stimulée de rayonnement ».
Le 1er laser a été mis au point aux Etats Unis en 1960 par Théodore
H. Maiman. Il s’agissait d’un laser à rubis mais dès l’année suivante était
construit le laser à gaz. De nos jours, le laser s’est développé
considérablement et ses applications sont nombreuses aussi bien du coté militaire
que du coté médical. C’est ce dernier point dont on va développer le sujet.
1. Principe général
Les électrons qui gravitent autour d’un atome ne peuvent décrire que des orbites de rayon déterminé, correspondant à des niveaux d’énergie d’autant plus élevés que ce rayon est plus grand. Lorsque, sous une action quelconque (par exemple une élévation de température), un de ces électrons passe sur une orbite plus éloignée du noyau, l’atome est alors dans un état excité ; l’opération est appelée pompage, par analogie avec le travail d’une pompe. L’atome peut revenir de lui-même à l’état neutre ; il émet alors, sous forme d’un photon, un rayonnement dont la fréquence f est proportionnelle à l’énergie mise en jeu.
Mais l’atome excité revient plus facilement à l’état neutre sous l’action d’un photon de même fréquence f, ce qui fait deux photons, capables à leur tour de désexciter deux autres atomes ; il en résulte une émission en chaîne d’un très grand nombre de photons sous l’action d’un seul, dans un milieu actif, c’est-à-dire contenant un nombre convenable d’atomes excités, tel est le principe du laser.
Le laser ainsi produit est en fait une onde électromagnétique qui a la principale caractéristique de pouvoir se propager dans le vide et de se déplacer en ligne droite dans les milieux homogènes. Ce type d’ondes couvre un large spectre auquel correspondent des longueurs d’ondes s’étalant de quelques kilomètres à quelques centièmes d’Angstrom. Elles sont caractérisées par deux paramètres essentiels :
- La puissance de l’émission, mesurée en watts, qui est un paramètre quantitatif.
- La fréquence (inverse de la longueur d’onde), mesurée
en hertz, qui est un facteur qualitatif : chaque fréquence correspond à
une couleur particulière.
Fréquences et longueurs d’ondes des rayonnements électromagnétiques
|
Type d’onde |
Fréquence |
Longueur d’onde |
|
Rayons gamma |
>3.1020 Hz |
< 0,001 nm |
|
Rayons X |
3.1019 Hz à 6.1017
Hz |
0,01 à 5 nm |
|
Ultraviolets |
3.1016 Hz à 8.1014
Hz |
10 à 400 nm |
|
Lumière visible |
3.1014 Hz à 4.1014
Hz |
400 à 800 nm |
|
Infrarouges |
4.1014 Hz à 3.1012
Hz |
800 à 15000 nm |
|
Radio-électriques |
Moins de 3.109 Hz |
Plus de 1 mm |
|
Hyperfréquence |
3.1011 Hz à 3.109
Hz |
1 mm à 10 cm |
|
Ondes courtes |
3.107 Hz |
10 m |
|
Ondes moyennes |
3.106 Hz |
100 m |
|
Grandes ondes |
3.105 Hz |
1 km |
2.Explications physiques
Tous les lasers sont composés d’un milieu actif excité par une source d’énergie, situé dans une cavité résonnante. Pour des raisons d’adaptabilités, on utilise des interfaces pour le transport du faisceau sauf pour de très rares cas.
a) Les milieux actifs
Le milieu actif peut être sous différents états tels
que :
-L’état solide (rubis, émeraude).
-L’état liquide (gaz carbonique).
-L’état gazeux (hélium-néon).
-L’état semi-gazeux (colorant).
Les molécules d’un milieu sont, dans les conditions
normales, à l’état fondamental. Pour devenir émetteur, ce milieu doit être
excité par un moyen approprié : l’énergie ainsi acquise par les atomes est
rapidement relarguée, soit par énergie calorifique ou en énergie cinétique,
soit, si l’excitation est suffisante, par émission de photons dont la fréquence
(la couleur) est fixée par la valeur des transitions électroniques
caractéristiques de l’atome excité : plus cette valeur est grande, plus la
fréquence émise est élevée.
L’émission spontanée des sources lumineuses naturelles
est incohérente, chaque atome se désactivant indépendamment au bout d’un temps
variable : les photons partent dans n’importe quelle direction. Par
contre, si un photon rencontre un atome excité dont l’énergie de désactivation
est égale à la sienne qui lui est propre, il provoque l’émission par cet atome
d’un photon induit : c’est l’émission
stimulée.
Pour que ce phénomène d’activation réciproque ait des
chances de se produire, il est nécessaire qu’un nombre considérable d’atomes
soient excités. La durée de vie des atomes ou molécules à l’état excité est
normalement d’environ 1 millionième de seconde pour les transitions
électroniques "permises". Mais ce temps peut être multiplié par un
facteur de 1000 à 1 million pour un autre type de transition, infiniment moins
probable, dite "interdite" : c’est à ce niveau "d’état
métastable" (presque stable) que, sous l’action d’un apport énergétique
intense et adéquat, des atomes d’un même degré d’excitation peuvent
s’accumuler. Cette inversion de population qui existe naturellement dans les
étoiles à des températures extrêmes, peut être réalisée grâce à un pompage
approprié, technique mise au point en 1950 par le Français Albert Kestler, prix
Nobel.
Toutefois, l’émission électromagnétique dont tous les
photons ont la même fréquence (monochromatique) se fait de façon désordonnée
car les photons sont émis dans n’importe quelle direction et à n’importe quel
moment. Par contre :
- Si on
emprisonne le milieu actif dans une cavité
limitée par deux miroirs se
faisant face, on introduit une boucle de rétroaction (feedback) dans
laquelle les ondes électromagnétiques font des allers et retours, avant de
pouvoir s’échapper par le miroir
dont l’indice de réfraction est légèrement inférieur à 100% (ce qui se
traduit par une légère transparence).
- Si on
ajuste la distance qui sépare les deux miroirs à un multiple de la demi-longueur
d’onde du rayonnement, les photons se propageant à l’intérieur de
l’oscillateur laser ainsi constitué provoquent, par résonance, la
transition harmonique à un niveau inférieur des électrons, des atomes
excités d’un même niveau énergétique : on obtient ainsi l’émission stimulée.
b) Les cavités
§
Les cavités à
miroirs plans :
L’obtention
d’une inversion de population importante est toujours difficile, et
l’amplification subie par l’onde lumineuse par unité de longueur est faible.
Cela conduit à construire des cavités longues, en séparant beaucoup les
miroirs. Or, le pompage exige généralement que l’une au moins des dimensions du
milieu amplificateur soit faible. Ce double impératif conduit à des cavités à
la fois longues et étroites, mettant en œuvre des miroirs largement séparés et
de faibles dimensions. Mais alors, un phénomène bien connu en
optique survient : la diffraction. Elle provoque à chaque réflexion de
l’onde sur les miroirs, son élargissement et toute l’onde ainsi renvoyée
n’atteint donc pas l’autre miroir, ce qui se traduit par des pertes
importantes.
Il
est donc très difficile de faire fonctionner un laser avec des miroirs plans,
et la quasi-totalité des lasers utilisent au moins un miroir sphérique concave
qui, à chaque passage de l’onde, la “ reconcentre » et réduit ainsi très
fortement les pertes par diffraction.
§
Les cavités à
miroirs sphériques
On montre que les
cavités à miroirs sphériques favorisent, tout comme les cavités à miroirs
plans, certaines ondes, qui en sont les modes.
Mais
ces modes ne sont plus les ondes planes se propageant en faisceaux parallèles,
caractéristiques des miroirs plans. Ce sont des faisceaux dits “
gaussiens », caractérisés par le fait que, à l’intérieur de leurs
sections, l’amplitude du champ lumineux E obéit à une loi qui est une loi
de Gauss : ![]() , r étant la distance à l’axe où le champ passe par sa valeur
maximale E0 ; et w est la mesure du rayon de la section transversale.
, r étant la distance à l’axe où le champ passe par sa valeur
maximale E0 ; et w est la mesure du rayon de la section transversale.
On
note que, de part et d’autre d’une section de diamètre minimal 2 w0, appelée le “ col » ou la “
taille » du faisceau, celui-ci se dilate selon la loi :  , z étant la distance à la taille.
, z étant la distance à la taille.
§
Modes des
cavités à miroirs sphériques et faisceaux gaussiens
C’est
l’existence de surfaces d’onde sphérique qui fait que les faisceaux gaussiens
sont des modes des cavités à miroirs sphériques. En effet, si l’on imagine,
dans un faisceau gaussien, deux surfaces d’ondes quelconques remplacées par des
surfaces réflectrices, il est aisé de voir que, chacune renvoyant l’onde
exactement sur elle-même, celle-ci va osciller indéfiniment entre ces miroirs,
en se retrouvant – à une atténuation près – identique à elle-même
après chaque aller et retour : la définition d’un mode.
À
l’inverse, si l’on se donne deux miroirs de courbure R1 et R2, séparés d’une
longueur d, tout faisceau gaussien
possédant, avec ce même écart, deux surfaces d’onde ayant ces courbures R1 et
R2 sera un mode de la cavité formée par ces miroirs. On montre que l’on peut
toujours trouver un tel faisceau à condition que R1, R2 et d respectent la double condition :  , ce qui signifie que ces miroirs peuvent alors constituer la
cavité d’un laser. L’intérêt des cavités sphériques est leur commodité de
réglage et elles sont très utilisées.
, ce qui signifie que ces miroirs peuvent alors constituer la
cavité d’un laser. L’intérêt des cavités sphériques est leur commodité de
réglage et elles sont très utilisées.
Cependant, si le gain de
l’amplificateur est élevé, on peut s’affranchir de la condition ci-dessus, en
constituant ce que l’on appelle une “ cavité instable ». Dans celles où
l’élimination des modes transverses est facile, le même résultat peut être obtenu
en conférant à l’un des miroirs un coefficient de réflexion décroissant du
centre au bord, selon une loi, par exemple, gaussienne.
3. Caractéristiques
des lasers :
Les
nombreux va-et-vient effectués par les photons dans la cavité résonnante
engendrent une directivité presque parfaite à la lumière c’est-à-dire que le
faisceau émis est très étroit et les rayons sont pratiquement parallèles. Ces
spécificités ne sont cependant pas les seules caractérisant les lasers, en
effet la puissance de l’émission varie beaucoup selon la nature du milieu
actif et la construction du laser. Et cette émission peut se faire de
différentes manières :
- Continue : lorsque
le pompage est constant (puissance constante).
- Impulsionnelle : le
pompage est intermittent (l’énergie, relâchée en un temps très bref (» 100 ms), est beaucoup plus
élevée que pour une émission continue).
- Déclenchée : un
mécanisme appelé “ Q-SWITCH » empêche l’énergie de s’échapper
(énergie relâchée en un temps encore plus bref que la précédente (» 10 ns) et la puissance
crête est d’autant plus élevée).
- Bloquée :
rayonnement émis en train d’impulsions dont la durée est de quelque
dizaines de picosecondes et dont la puissance crête peut dépasser 10
gigawatts.
4. Les types de
lasers :
Depuis
le découverte du 1er laser, plusieurs centaines de types de lasers
ont été réalisés fonctionnant à des longueurs d’ondes couvrant de l’infrarouge à
l’ultraviolet. Ils utilisent des milieux actifs très variés, souvent réalisés
par le mélange d’un composant principal neutre et d’une impureté
activatrice : c’est le dopage. Ils reposent sur le même principe de base
mais diffèrent par leur puissance, leur fréquence, la propriété de leur
faisceau... On peut les classer en 3 catégories :
- Les lasers
solides constitués d’un cristal ou d’un verre dopé.
- Les lasers à liquide.
- Les lasers à gaz.
a) Les lasers
solides :

Le laser à rubis : Il
émet dans le rouge foncé (lointain) à 692,7 et surtout à 694,3 nm et est le
laser le moins utilisé actuellement. Le pompage est réalisé par une ou deux
lampes flashes au xéon avec une enveloppe en quartz pour laisser passer les
ultraviolets qui sont absorbés par le cristal tout comme les rayons lumineux.
Il fonctionne sur le mode impulsionnel et peut atteindre une puissance de 100
Watts.
Le laser Néodyme-Yag : Il émet
dans l’infrarouge proche à 1064 et 1318 nm. C’est le plus répandu des lasers
solides. Le pompage se fait soit par
une ou plusieurs lampes à arc, soit par des flashes à gaz rares, soit par
d’autres lasers, semi-conducteurs en particulier, le tout enserré dans une
cavité réflectrice de façon à concentrer le maximum d’énergie sur le barreau.
Il fonctionne soit sur le mode impulsionnel avec des durées d’impulsions
d’environ 50ms, soit sur le mode déclenché ou bloqué qui permet d’atteindre
durant des temps très brefs des énergies énormes.
Le laser à Alexandrite : Il
émet dans le rouge entre 700 et 800 nm. Son émission stimulée est couplée à une
vibration du réseau cristallin qui a pour effet d’élargir la bande d’émission.
Ce laser est beaucoup moins utilisé que le YAG et sa puissance est plus limitée
(3 Watts en continu mais près de 20 mégawatts-crête en impulsionnelle).
Le laser à semi-conducteurs : Il émet selon sa composition dans l’infrarouge proche et
le rouge. Il utilise en pompage le courant électrique et son rendement
excellent permet de l’exciter par de simples piles. Cependant sa puissance est
limitée à quelques dizaines voire quelques centaines de watts. Il a un grand
avenir dans les télécommunications par fibres optiques.
b) Les lasers à
liquide :
Du fait que de nombreux composés organiques absorbent
efficacement certains rayonnements et présentent à l’état liquide une
fluorescence intense qui couvre généralement une large bande située dans le
visible, on peut sélectionner à l’aide d’un prisme une longueur d’onde
particulière.
Le milieu actif est composé de divers colorants dont
chacun à une bande de fréquence qui lui est propre.

Le pompage peut
être réalisé par flash. Dans ce cas le liquide est placé dans un tube, le
colorant est projeté sous forme d’un jet extrêmement fin sur lequel le faisceau
d’un laser émet à une fréquence efficacement absorbée par le milieu actif et
est braqué selon l’angle le plus favorable (où la réflexion est minimale) ou
angle de Brewster.
c) Les lasers à
gaz :
Ils sont tous constitués d’un tube contenant le gaz
excitable dont les extrémités sont soit transparentes, soit réfléchissantes.
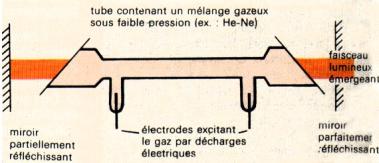
Laser à Hélium-Néon : Ce fût le 1er
laser émettant en continu. Il émet dans le rouge à 632,8 nm, son émission est
très pure et sa puissance ne dépasse pas les 50 mW. Le pompage est électrique,
l’excitation porte sur le néon et le refroidissement se fait par air.
Laser à
argon et krypton ionisés : Ces gaz perdent facilement un électron sous
l’action d’une décharge électrique et les atomes ainsi ionisés constituent le
milieu actif. L’argon ionisé a une émission continue ou en train d’ondes très
brèves (sa puissance peut atteindre 20 W avec des raies sélectionnables, dans
le bleu à 488 nm et dans le vert à 514,5 nm). Le krypton, quant à lui, émet
dans le rouge et le jaune et sa raie la plus intense peut atteindre 647,1 nm.
Le refroidissement se fait par l’eau.
Laser à
vapeur métallique : A de très hautes
températures, on peut obtenir des vapeurs d’un certain nombre de métaux qui
peuvent permettre la réalisation d’un laser. Il peut émettre dans le bleu (or),
dans le vert (cuivre, manganèse) ou
dans le rouge (or, plomb). Ce laser est impulsionnel avec des taux de
répétition très élevés et sa puissance dépend du diamètre du tube.
Laser à
gaz carbonique : Il émet dans l’infrarouge lointain, principalement à 10,6 nm. Sa
puissance peut atteindre en continu 300 W et plusieurs kilowatts en impulsions.
Son alimentation se fait par décharges électriques, son refroidissement se fait
par eau ou huile.
Laser à azote : C’est le
1er laser dont une émission dans l’ultraviolet a été observée. Il
émet par impulsions brèves (1 à 10ns) ce qui fait que sa puissance est très
limitée.
Laser à excimères : C’est un
laser dont le milieu actif est constitué de molécules diatomiques n’existant
qu’à l’état excité résultant d’une réaction que l’on peut provoquer par des décharges électriques sous
haute pression entre gaz rares (argon, krypton, xénon), ainsi qu’entre gaz
rares et halogènes (fluor, chlore, brome, iode) ou oxygène et gaz rares (oxyde
de xénon). Parmi la vingtaine de molécules, le fluorure de krypton et le
chlorure de xénon possèdent des performances similaires, ils émettent dans
l’ultraviolet et respectivement à 248
et 308 nm. Ils fournissent des impulsions d’une durée de 10 à 20 ns dont la
puissance crête est de plusieurs mégawatts, mais cela représente une puissance
moyenne de 25 W du fait de leur cadence de répétition élevée.
5. Les
interfaces :
Afin
de focaliser le laser sur un point minime ou, au contraire, de le disperser, on
utilise des interfaces dont les caractéristiques varient en fonction de leur
conception.
a) Le bras articulé à
miroirs :
Il
est essentiellement utilisé pour les lasers CO2 et fonctionne sur le
principe de la réflexion sur des miroirs (généralement au nombre de 7) disposés
dans les coudes d’un bras articulé. Ce système exige une mécanique précise, ce
qui le rend assez fragile et surtout onéreux. Cependant il a l’avantage de
conserver au faisceau toutes ses qualités optiques. Au bout du bras se trouve
une sorte de stylo optique comportant diverses lentilles de focalisation
interchangeables en matériau transparent au rayonnement émis ce qui permet au
chirurgien une bonne prise en main.
b) Les fibres
optiques :
Elles
constituent un moyen de transmission quasiment idéal pour la majorité des
lasers sauf les lasers à CO2 car les fibres actuelles ne sont pas
suffisamment transparentes aux infrarouges lointains. Il en existe plusieurs
types mais seule la “ monofibre multimodale à saut d’indice », dont le
coeur en silice est entouré d’une gaine en silicone ou en silice dopée dont
l’indice de réfraction est plus faible, est utilisée en milieu médical. Cette
conception permet ainsi au rayon lumineux de passer lorsqu’on courbe la fibre
car lorsqu’un rayon lumineux est incliné sur l’axe, il est renvoyé au coeur de
la fibre par réflexions successives coeur/gaine. Toutefois, elle n’est pas
exempte de défaut car le faisceau qui en émerge est légèrement divergent et a
perdu une partie de sa cohérence initiale.
Le
coeur de la fibre est selon l’application de 200, 400 ou 600 µm et celui de la
gaine n’excède pas 1 mm ce qui permet une grande flexibilité. Les fibres
optiques peuvent être utilisées nues mais, en raison de leur fragilité, elles
sont le plus souvent protégées par une gaine en téflon et éventuellement
refroidies du fait du possible échauffement du coeur avec la puissance du
rayonnement. En général, on adapte en bout de fibre une pièce à main dont le
type diffère selon les usages.
c) Les endoscopes :
Ce
sont des tuyaux de différents diamètres comportant un système d’éclairage, un
système d’observation et un canal opérateur. Ils peuvent être rigides ou
souples avec une extrémité orientable au moyen de câbles actionnés depuis la
poignée de commande. L’éclairage et l’observation se font alors par des fibres
optiques très fines. Certains modèles comportent des système d’insufflation de
gaz et d’aspiration ou d’injection de liquide et ils peuvent être couplés à une
caméra pour projection du champ opératoire sur écran de télévision. L’adaptation
des lasers ne pose pas de problème car on utilise le canal opérateur pour faire
la visée ou pour introduire la fibre optique préalablement stérilisée.
d) Les microscopes
opératoires :
Ce
sont des microscopes binoculaires stéréoscopiques à grossissement réglable qui,
couplés à un micromanipulateur, permettent des dissections fines irréalisables
directement. Montés sur différents systèmes endoscopiques pour une chirurgie
non invasive, ils permettent l’examen direct et l’intervention au niveau des
structures telles que le cerveau, l’abdomen, les articulations et de cavités
comme le larynx et les bronches, le tubes digestif, le système uro-génital ou
vasculaire.
Un
boîtier permet d’adapter le bras articulé ou la fibre du laser sur le
microscope, et un système optique assure la focalisation du faisceau et la
visée dans le champ de vision du microscope.
e) La lampe à
fente :
Elle
est surtout utilisée en ophtalmologie, analogue au microscope opératoire mais
comportant un système d’éclairage particuliers
qui projette, selon différents angles, une raie lumineuse de couleur et de
largeur réglable à l’intérieur du globe oculaire du patient, non seulement pour
en faire un examen complet, mais également pour en évaluer la courbure.
Le
faisceau du laser, généralement à argon, est transmis le plus souvent par une
fibre optique et orienté à l’aide d’un miroir et d’une manette permettant de
diriger à distance le faisceau lumineux du laser appelée palonnier. Un zoom
permet de régler le diamètre de l’impact (entre 50µm et 1 mm).
II- Les lasers et le milieu médical
1. Les effets
biologiques du laser :
Les
effets biologiques du laser dépendent de plusieurs paramètres :
- La fréquence de
l‘émission.
- L’intensité de
l’émission.
- Le mode temporel
(continu ou discontinu) de l’émission.
a) La fréquence :
Elle
détermine le niveau de l’intéraction entre le rayonnement et la matière qui ne
dépend que de la quantité d’énergie véhiculée par chaque photon, c’est-à-dire
que plus cette quantité est grande plus la fréquence est élevée. Les effets
biologiques sont propres à une fréquence donnée. En effet, les
rayonnements :
- infrarouges augmentent
l’énergie vibratoire des molécules.
- visibles provoquent des
transitions au niveau des électrons des couches atomiques externes sans
être destructrices pour des puissances absorbées n’élevant pas la
température des tissus au-delà des limites physiologiques.
- ultraviolets, X et
gamma agissent sur l’intimité même des molécules car ils éjectent des
électrons hors des molécules (effet ionisant), désorganisant ainsi les
structures chimiques. Cependant, pour déclencher une réaction biochimique
dans ces conditions, il faut une intensité de rayonnement suffisante à la
fréquence favorable : seul les lasers, qui véhiculent des flux photoniques
intenses, sont capables de concentrer de telles énergies en un point
précis, grâce à leurs caractéristiques exceptionnelles (monochromaticité
(émission dans une gamme très étroite de fréquences), cohérence (permet
d’additionner les énergies de plusieurs photons en un temps extrêmement
court), directivité).
b) L’intensité :
Elle
conditionne la quantité d’énergie absorbée par unité de surface et de temps. La
profondeur de pénétration du rayonnement est fonction du pourcentage d’énergie
dissipée par unité de longueur (facteur volume), pourcentage variable selon
l’absorption du tissu irradié, spécifique de la fréquence de l’émission. Ces
paramètres conditionnent l’effet calorifique recherché en photochirurgie,
d’autant plus intense que le rayonnement est rapidement absorbé. Cette action
dépend également du mode temporel de l’émission, ainsi que de la
vascularisation du tissu considéré.
c) Le mode
temporel :
Il
influence également son effet biologique. Des expérimentations ont montré que
les émissions pulsées ont des effets biochimiques plus marqués que les
émissions continues, pour des intensités moyennes semblables ou inférieures.
Les tissus réagissent à la fois, aux rayonnements d’une façon spécifique ou
aspécifique, ainsi qu’aux variations propres du champ électromagnétique. Tous
les systèmes semblent sollicités, y compris les acides nucléïques des noyaux
cellulaires. Avec les lasers “ déclenchés » ou “ bloqués », on
obtient des impulsions extrêmement brèves et des densités de flux considérables
qui créent un plasma et une onde de choc extrêmement localisés, susceptibles de
désintégrer les structures moléculaires du milieu récepteur même s’il est
transparent au rayonnement : cela est particulièrement intéressant en
ophtalmologie.
2. Action du laser
sur un milieu :
Lorsqu’un
rayonnement est dirigé, à partir d’un milieu initial (air ou fibre optique),
sur un milieu dont l’indice de réfraction est différent (comme un tissu
biologique), une partie du rayonnement est réfléchie à l’interface et l’autre pénètre
dans le milieu. Deux phénomènes se produisent au niveau du rayonnement
transmis : il y a réfraction des rayons qui abordent la surface de
séparation en oblique et absorption d’une partie du rayonnement par les
molécules du milieu, dont l’énergie est de ce fait augmentée.
Les tissus biologiques étant très inhomogènes, les
phénomènes de réfraction sont particulièrement marqués, entraînant une diffusion importante et rendant rapidement
le faisceau très divergent. Ces phénomènes sont communs à toutes les fréquences
d'ondes électromagnétiques.
a) L'absorption :
Elle est conditionnée par la fréquence : chaque molécule
a un “ spectre » d'absorption qui lui est propre. La transparence des tissus
biologiques diminue progressivement des ondes hertziennes (ondes radio) aux
infrarouges, alors qu'elle augmente à partir des ultraviolets jusqu'aux rayons
gamma. Cela est dû à la richesse en eau de ces tissus (70 % environ du poids du
corps humain) : l'absorption des ondes électromagnétiques par l'eau croit
rapidement de la gamme des ondes longues jusqu'aux infrarouges. Après un
maximum dans l'infrarouge lointain, on assiste à un effondrement dans l'infrarouge
proche et le visible, correspondant, dans notre environnement terrestre chargé
d'humidité, à une “ fenêtre atmosphérique » de propagation dans laquelle la
transparence maximale se place autour de la couleur jaune‑vert (ce qui
permet l'ensoleillement de notre globe). Immédiatement au‑delà, dans
l'ultraviolet, le coefficient d'absorption culmine à un niveau très élevé avant
de décroître pour les fréquences X et gamma.
Pour cette raison, le puissant rayonnement du laser CO2,
qui émet dans l'infrarouge lointain, est fortement absorbé par l'eau : il
volatilise les tissus et donne une coupe fine et rapide dont la profondeur,
limitée à 2 millimètres, est avantageuse en chirurgie.
Le rayonnement vert du laser argon traverse facilement
les milieux aqueux, mais est entièrement absorbé par l'hémoglobine du sang : il
photocoagule parfaitement les hémorragies superficielles et est bien adapté à
la destruction des tumeurs vasculaires (angiomes).
Par contre, les lasers au rubis et au néodyme, dont les
émissions intenses, respectivement rouges et infrarouges proches, sont bien
absorbées par les tissus mais peu par l'eau et le sang, sont préférables pour
maîtriser les hémorragies profondes. L'absorption par les pigments rétiniens de
tous les rayonnements visibles, contrairement aux parties antérieures de l'œil
(transparentes), représente des conditions favorables à l'emploi des lasers à
rubis, krypton et argon en Ophtalmologie.
b) La pénétration :
Elle est fonction de cet ensemble de facteurs:
- La
réflexion (facteur sur lequel on peut agir en dirigeant le rayon à angle
droit sur le tissu).
- La
réfraction (intense vu l'inhomogénéité des structures biologiques).
- L’absorption
(spécifique à chaque sorte de molécule, mais généralement forte en raison de la multiplicité des
éléments): seules les émissions rouges et infrarouges proches, peu
absorbées par l'eau et les pigments biologiques, pénètrent quelque peu
dans l'organisme (de l'ordre de quelques millimètres à 2 centimètres selon
les tissus considérés).
En effet, les os
fins laissent passer une certaine quantité de rayonnement alors que les
structures translucides, tels le tissu cartilagineux (pavillon de l'oreille)
ou les tendons, semblent moins transparents que d'autres tissus plus opaques
(muscles), sans doute parce que ces structures jouent le rôle de guide d'ondes
et réfléchissent l'émission longitudinalement; que les tissus glandulaires
(testicule) sont relativement perméables aux rayonnements laser et doivent être
biologiquement influençables par ces émissions.
3. Exemples d’utilisation des lasers :
a)
Ophtalmologie :
Il est logique que ce soit au niveau de l'œil,
récepteur privilégié de la lumière, que les premières applications médicales
des lasers aient été réalisées. L'utilisation des lasers à argon, et plus tard
à krypton, au néodyme-YAG en impulsions ultracourtes (mode bloqué) et à
excimères, a fait faire de grands progrès à l'ophtalmologie.
Applications thérapeutiques des lasers :
Les traitements par laser
ne s'adaptent qu'à une partie des maladies de la sphère oculaire: ils n'ont
actuellement aucune application intéressante au niveau de la paupière et de la
conjonctive.
Les affections de la
rétine ont été les premières à bénéficier des possibilités des émissions laser.
Les décollements de la rétine, provoquant une déchirure de la membrane, se
produisent le plus souvent chez les grands myopes et chez les sujets âgés dont
l'état vasculaire est médiocre, ou à la suite d'un traumatisme.
Le traitement, préventif
ou curatif, consiste à détruire ou à isoler la lésion en la cernant de trois ou
quatre rangées d'impacts laser juxtaposés, la coagulation des tuniques assurant
leur soudure.
Les lasers à argon, dont
les émissions vertes et bleues sont bien absorbées par les milieux pigmentés et
vasculaires du fond de l'œil, ont remplacé depuis deux décennies les premiers lasers
à rubis. L'élévation thermique, importante mais très localisée au niveau de
l'impact sur la rétine, est faible dans les milieux intra‑oculaires,
assurant une cicatrisation beaucoup plus rapide qu'avec les anciens arcs au
xénon. Enfin, la rapidité de l'opération et son caractère strictement indolore
permettent d'intervenir sur des patients non anesthésiés, et sans
hospitalisation.
Pour l'ablation chirurgicale du
cristallin, qui est nécessaire pour maintenir la vision lorsque les moyens
médicaux s'avèrent insuffisants, l’utilisation du laser néodyme-YAG en mode
bloqué (impulsions hyper puissantes de quelques picosecondes) permet
l'ouverture de la capsule antérieure du cristallin et ainsi faciliter
l'extraction.

Prospectives :
Les études s'orientent dans
trois sens:
1.
recherche de lasers de nouvelles longueurs d'onde.
2.
meilleure utilisation des lasers.
3.
scanners à lasers.
Les lasers à excimères,
tirant dans l'ultraviolet, permettent de réduire considérablement les effets
thermiques autour du point d'impact : les tissus sont littéralement volatilisés
sur place ce qui laisse une plaie extrêmement fine, dont les bords sont
parfaitement nets et réguliers (photoablation). On les utilise par exemple dans
les incisions parfaitement concentriques de profondeur déterminée permettant de
modifier la courbure de la cornée et de réduire la myopie.
La tomographie laser fournit des
images digitalisées, c'est‑à‑dire point par point, du nerf optique,
qui peuvent être reconstruites en trois dimensions a la manière d’un scanner
classique. Des prototypes d'appareils de ce type ont été récemment réalisés aux
États‑Unis. Ils sont au stade expérimental, mais s'avéreront certainement
très utiles pour évaluer objectivement l'état des nerfs optiques chez les
malades .
L'utilisation des lasers a
transformé la chirurgie ophtalmologique : les découvertes futures permettront à
coup sûr d'élargir encore le champ des possibilités thérapeutiques de ces
appareils “ de lumière », peut-être grâce aux lasers à colorants dont la
fréquence est “ accordable », peut-être par la représentation holographique (en
trois dimensions) du champ opératoire et le calcul informatisé, pour le
bénéfice et le confort des patients.
b) Dermatologie :
Depuis plusieurs année, un grand nombre d'applications
qui représentent un réel progrès en thérapeutique dermatologique ont été
codifiées. Et le laser à argon est le plus employé dans cette discipline.
- Lésions
cutanées :
Les angiomes, qui sont des tumeurs plus ou moins bien
individualisées constituées par l'agglomération de vaisseaux sanguins ou
lymphatiques (ils se développent fréquemment sur le visage et posent un
problème esthétique), sont de nos jours traités par le laser à argon dont
l'émission est sélectivement absorbée par l'hémoglobine du sang. Ce traitement
laser est généralement réalisé par coagulation des lésions point par point, à
la pièce à main. Les puissances utilisées sont de l'ordre de 2 watts par
millimètre carré, en impacts de 0,2 seconde. Ainsi les tissus sains, épiderme
et annexes, relativement transparents au rayonnement, sont peu concernés par
les effets thermiques, ce qui assure, en règle générale, une bonne
cicatrisation. Cependant, les traitements aux lasers à argon sont limités par
l'épaisseur et la couleur des lésions car leur émission n'intéragissent avec
les tissus qu'en fonction de son absorption.
Des tentatives de traitement avec d'autres types de
lasers ont été faites. Le laser au rubis pulsé offre deux avantages : son
émission, très brève, est pratiquement indolore. Le diamètre de ses spots,
beaucoup plus important que celui de l'argon, permet des traitements de larges
surfaces en un seul temps. Il peut être utilisé seul, ou conjointement au laser
à l'argon dans le traitement des angiomes
 Les lasers à colorants
ont les mêmes avantages que les lasers a rubis, avec en plus la possibilité
d'optimaliser la longueur d'onde de l'émission en fonction du spectre
d'absorption maximum de la lésion (585 nm pour un angiome). En régime pulsé
(impulsions de 300 à 500 microsecondes), leur spot lumineux, d'un diamètre de
plusieurs millimètres, n'attaque pas l'épiderme : la cicatrice n'est donc
jamais dystrophique. Ils ne sont toutefois efficaces que sur les vaisseaux dont
la lumière est inférieure à 80 micromètres, ce qui rend plusieurs passages
nécessaires sur la même zone pour obtenir un palissement notable. Mais leurs
tirs sont à ce point indolores qu'ils sont facilement utilisables chez les
jeunes enfants. Une technique de gestion du laser et de balayage automatique
par pièce à main robotisée (Hexascan) a été mise au point par Jean‑Marc
Bruneteaud et Serge Mordon : elle assure une plus grande rapidité de traitement
et une meilleure uniformité cicatricielle, mais est encore peu répandue.
Les lasers à colorants
ont les mêmes avantages que les lasers a rubis, avec en plus la possibilité
d'optimaliser la longueur d'onde de l'émission en fonction du spectre
d'absorption maximum de la lésion (585 nm pour un angiome). En régime pulsé
(impulsions de 300 à 500 microsecondes), leur spot lumineux, d'un diamètre de
plusieurs millimètres, n'attaque pas l'épiderme : la cicatrice n'est donc
jamais dystrophique. Ils ne sont toutefois efficaces que sur les vaisseaux dont
la lumière est inférieure à 80 micromètres, ce qui rend plusieurs passages
nécessaires sur la même zone pour obtenir un palissement notable. Mais leurs
tirs sont à ce point indolores qu'ils sont facilement utilisables chez les
jeunes enfants. Une technique de gestion du laser et de balayage automatique
par pièce à main robotisée (Hexascan) a été mise au point par Jean‑Marc
Bruneteaud et Serge Mordon : elle assure une plus grande rapidité de traitement
et une meilleure uniformité cicatricielle, mais est encore peu répandue.
De nombreuses autres lésions cutanées à composante
vasculaire ont pu ainsi être abordées avec succès.
- Tumeurs
cutanées :
Les verrues vulgaires, certaines tumeurs superficielles
bénignes, les végétations vénériennes (crêtes de coq) qui siègent sur les
organes génitaux externes, à la marge anale, dans le vagin ou sur le col utérin,
classiquement détruites par électrocoagulation, sont plus facilement traitables
par les lasers à argon, au CO2 ou néodyme‑YAG qui ont l'avantage de la
rapidité d'action, de la meilleure qualité de cicatrisation, de l'absence
d'hémorragie et du moindre pourcentage de récidive.
c) Chirurgie
générale :
Les qualités de coupe et de coagulation des lasers ont
rapidement intéressé les chirurgiens mais ces propriétés, en rapport avec l'effet
thermique résultant de l'absorption de l'énergie lumineuse par les tissus, ne
sont pas uniformément réparties parmi les lasers : même pour détruire, il faut
faire la part du qualitatif autant que du quantitatif.
Au‑dessus de 44 degrés
centigrades, les tissus se rétractent : entre 60 et 80 degrés ils sont coagulés
et au‑delà, ils sont carbonisés, et vers 100 degrés, volatilisés. Selon
la sélectivité de l'absorption par les divers composants des tissus, l'action
prépondérante est soit la coupe, soit la coagulation en surface ou en
profondeur.
- Les
fréquences d’émission :
L'émission infrarouge des puissants lasers au CO2 est
fortement absorbée par l'eau, qui constitue environ 70 % du poids du corps
humain : elle volatilise les tissus, ce qui donne une coupe nette et fine de 1
à 2 millimètres de profondeur, mais n'empêche pas l'hémorragie des tissus
vascularisés. Son rayonnement étant invisible, il est nécessaire, pour que le
chirurgien puisse ajuster son geste, de l'accompagner d'une émission lumineuse de
même axe : c'est, en pratique, un laser hélium‑néon de faible puissance
qui sert de viseur.
Par contre, les lasers à l'argon (vert et bleu), au
krypton (jaune et rouge), au rubis (rouge foncé) et au néodyme (infrarouge
proche, donc invisible), dont l'émission pénètre plus profondément dans les
tissus, ont un effet thermique moins localisé : ils coagulent mieux, mais
donnent une coupe moins précise que le laser au CO2.
L'argon, très absorbé par le sang, est le plus performant
pour les hémorragies de surface. Il nécessite 4 à 5 fois moins de puissance que
le néodyme‑YAG pour obtenir un même effet, mais il est impuissant sur des
vaisseaux dont la lumière excède 0,5 millimètre. Par contre, le YAG, dont
l'action prépondérante se situe au niveau des protéines, assure une hémostase
(arrêt d'hémorragie) plus profonde et permet la coagulation de vaisseaux de 2
millimètres de diamètre.
Le choix est donc délicat et difficilement parfait. Seul
le laser CO2, véritable scalpel optique, est apte à remplacer le classique bistouri
dans certains gestes de chirurgie générale, alors que l'argon ou le néodyme‑YAG,
selon les cas, peuvent avantageusement évincer l'électrocoagulateur (bistouri
électrique). Mais ceci représente, dans le bloc opératoire, deux gros appareils
bien embarrassants.
Le CO2, dont les émissions ne passent pas à travers les
fibres optiques qui équipent les autres lasers, doit être couplé à un bras
articulé, aussi loger et maniable que possible, et équipé d'une pièce à main à
focales interchangeables. Le geste chirurgical, modifié par le manque de
contact avec la plaie opératoire, devient très complexe pour un système multi‑lasers,
le chirurgien n'ayant que deux mains, sans parler du coût de l'installation.
Les lasers ont toutefois des avantages décisifs : ils permettent
d'effectuer des opérations de coupe, de destruction et d'hémostase, sans
contact avec les tissus, ce qui limite les risques d'infection secondaire. De
plus, leurs émissions sont aseptisantes par effet calorifique : les microbes
éventuellement présents sont détruits en même temps que les tissus.
- Utilisations
chirurgicales :
Les lasers à CO2, au Nd : YAG et à argon (souvent trop
peu puissant) sont les seuls à être utilisés actuellement en chirurgie
générale.
Par un paradoxe apparent, la chirurgie des grands brûlés
a été une des premières à profiter des avantages du laser. En permettant, sans
le moindre contact, l'excision précoce des tissus nécrosés avec stérilisation
de la plaie sous‑jacente, le rayonnement CO2 active la cicatrisation des
zones atteintes, réduit les pertes sanguines et les exsudations qui
affaiblissent le patient. Donc des greffes de peau, qui ne prennent que sur une
surface saine, peuvent alors être pratiquées dans des délais beaucoup plus
brefs et dans de meilleures conditions.
L'utilisation simultanée d'un rayonnement CO2 et d'un
rayonnement néodyme-YAG, focalisés sur un même point et pilotés par un faisceau
coloré provenant d'un laser hélium‑néon ou argon de faible puissance, a
transformé les données de la chirurgie au laser. Grâce à cette méthode on
obtient une coupe rapide, parfaite, et une hémostase instantanée. Cela permet
de pratiquer des résections partielles d'un organe aussi vascularisé que le
foie avec un minimum d'effusion sanguine, et d'éviter ou tout au moins de
limiter considérablement les transfusions importantes, avec les risques que
cela implique, nécessitées par les techniques classiques.
Aujourd’hui les appareils sont des montages compacts,
commercialisés, réunissant les deux lasers chirurgicaux et le laser de guidage
sous un même habillage (Combo‑laser).
Il est probable que cette innovation, particulièrement
précieuse lorsqu'il faut intervenir sur un tissu qui saigne abondamment ou qui
risque de disséminer des cellules malignes ou parasitées, sera rapidement
favorable à la multiplication des utilisations de ces appareils en grande
chirurgie.
d) Neurochirurgie :
Les premières applications des lasers en neurochirurgie
eurent lieu en 1976, avec le CO2, puis, en 1980, avec le néodyme‑YAG.
- Les
contraintes :
- Nécessité d'éviter
un sacrifice délibéré de tissu cérébral qui ne se reconstitue pas.
- Obligation de ne pas léser les zones spécialisées de la
couche externe du cerveau (cortex) sous peine d'entraîner des dommages
définitifs.
- Nécessité de préserver la circulation cérébrale durant
l'opération, d'éviter l'hémorragie post‑opératoire,
susceptible de provoquer une compression redoutable dans la cavité non
expansive qu'est la boîte crânienne.
- Apport
des lasers :
Face à ces contraintes anatomiques et physiologiques, la neurochirurgie
moderne a bénéficié d'importants progrès techniques, au premier rang desquels
se placent, très certainement, les lasers : ils permettent de réaliser, grâce à
leurs propriétés thermiques, tout à la fois la vaporisation, la section et la
coagulation. De plus, leur rayonnement peut être facilement dirigé à travers le
microscope opératoire branché sur un endoscope, quotidiennement utilisé en
neurochirurgie.

Les lasers ont
ainsi considérablement amélioré la sécurité des opérations sur le cerveau,
l'absence de contact entre l'instrument et le tissu diminuant le risque de
blessure de structures fonctionnellement importantes. Ils permettent de
réaliser des interventions considérées jusqu'à présent comme périlleuses voire
irréalisables, où s'accompagnant à coup sûr de dommages irréversibles.
Laser Néodyme YAG 30W 3mJ 1064 nm Utilisé pour le traitement des
tumeurs au cerveau
- Laser
et tissu cérébral :
Le parenchyme cérébral est un tissu mou, non pigmenté,
riche en eau. Il est donc logique que les émissions des lasers à CO2, qui
interagissent fortement avec l'eau, soient beaucoup plus rapidement absorbées
(en moins de 1 millimètre) que celles des néodyme-YAG qui pénètrent à environ 8
millimètres. Les qualités et les inconvénients de chacun de ces lasers sont
valorisés par ces caractéristiques.
- Les
avantages du CO2 sont :
- Section précise avec effet thermique spatialement
réduit
- Possibilité de vaporisation des tumeurs solides
- Absence d’œdème post‑opératoire
- Raccourcissement du temps opératoire
- Manipulation non invasive grâce au microscope
opératoire et précise par micromanipulation.
- Ses
inconvénients sont :
- Faible pouvoir hémostatique
- Augmentation de la durée de destruction des tumeurs
volumineuses (de plus de 3 à 5 centimètres)
- Risque de blessure de parties nobles en cas de
déplacement du spot par inadvertance en raison de la puissance du rayonnement.
- Les
avantages du néodyme-YAG sont :
- Remarquable effet d'hémostase sur les hémorragies en
nappe
- Coagulation de vaisseaux jusqu'à 2 millimètres de
diamètre
- Possibilité de résection de malformations vasculaires
- Utilisation très pratique grâce aux fibres optiques.
- Ses
inconvénients :
- Section parenchymateuse difficile
- Vaporisation peu efficace
- La puissance utilisable étant limitée par les effets
thermiques en profondeur.
- Application
des lasers en neurochirurgie :
La chirurgie cérébrale est dominée par le traitement des
tumeurs, des hémorragies et des troubles vasculaires.
Les propriétés des lasers à CO2 sont essentiellement exploitées
pour l'exérèse des tumeurs solides, cancéreuses ou bénignes.
Le laser au néodyme-YAG est préféré pour la destruction
de tumeurs profondes ou d'abord difficile (son rayonnement, vehiculable par
fibre optique, est plus facilement dirigé dans des endroits peu accessibles),
dures et saignantes, pour le traitement des hémorragies en nappe ou encore des
sutures vasculaires.
L'intérêt des lasers à argon est limité, par sa puissance
trop faible, à l'ablation des tumeurs cérébrales molles, des tumeurs de la
moelle épinière, et à la section sélective des racines postérieures
(sensitives) de certains nerfs rachidiens dans le traitement de douleurs
irréductibles.
e) Oto‑rhino‑laryngologie :
Cette spécialité ne concerne que des cavités (oreilles,
nez, gorge, larynx) dont l'examen nécessite des instruments spéciaux. Les
anciens outils sont de nos jours remplacés, pour les actes opératoires, par des
endoscopes rigides ou souples (fibroscopes), le plus souvent couplés à un
microscope opératoire, à une caméra projetant l'image sur un écran de
télévision, et à divers instruments de mesure.
Les émissions laser peuvent être véhiculées soit par
miroirs orientables pour le laser à CO2, soit par fibres optiques pour les
autres lasers, à travers des endoscopes adaptés à chaque organe. L'ORL a été
une des premières spécialités à bénéficier de ces progrès ainsi que des
traitements par laser.
- Bouche
et pharynx :
Dans le domaine des cancers de la cavité buccale, les
lasers habituels n'ont qu'une valeur palliative ou de confort, dans le but de
réduire le volume de tumeurs buccales qui ont une fâcheuse tendance à
disséminer. Le laser à colorant peut dans certains cas, couplé à certains
composants chimiques, réaliser une cure spécifique.
Un traitement ambulatoire a été appliquer pour lutter
contre le ronflement. En effet le ronfleur est un asphyxique qui s’ignore. Le
ronflement s'accompagne d'arrêts respiratoires, plus ou moins fréquents et plus
ou moins prolongés, ce qui entraîne une sous‑oxygénation, en particulier
cérébrale et cardiaque, facteurs de fatigue et de somnolence. Le traitement est
basé sur une résection progressive du voile du palais et de ses attaches en
fond de gorge (piliers postérieurs) au laser à CO2 de faible puissance (10 à 20
watts), sous simple anesthésie par pulvérisation locale (spray), afin de
réaliser un élargissement progressif de l'isthme pharyngé. Cette méthode ne
provoque jamais d'hémorragie si ce n’est que de légères «douleurs d'angines »
vite calmées.
- Pathologie
laryngée :
C'est la pathologie laryngée qui a le plus bénéficié des indications du
laser, tant dans les troubles de la voix que dans les états précancéreux ou
cancéreux et les sténoses laryngo‑trachéales.
Il n'est malheureusement pas possible, de nos jours,
d'employer le fibroscope souple pour les interventions sur le larynx, car les
rayonnements laser transmissibles par fibre optique (néodyme‑YAG ou
argon) sont trop pénétrants : ils léseraient les muscles des cordes vocales et
altéreraient définitivement la voix. Seul le laser à CO2 émettant en continu,
relié par bras optique à un laryngoscope rigide couplé à un biomicroscope, est
utilisable.
Certaines affections ont vu leur traitement et leur
pronostic totalement modifiés par l'emploi du laser. Comme pour la
papillomatose laryngée chez les enfants, maladie bénigne mais très récidivante,
caractérisée par la prolifération de petites tumeurs pédiculées. Le traitement
repose sur la vaporisation des lésions au laser à CO2, ce qui permet une
exérèse sans saignement et une récupération anatomique parfaite, au prix d'une
simple hospitalisation de 48 heures. Il y a aussi les paralysies laryngées qui
sont le plus souvent responsable d’une atteinte des nerfs moteurs des cordes
vocales (nerfs récurrents), et qui entraîne une fermeture de la glotte : le
laser ne peut prétendre à en traiter la cause, mais constitue un moyen simple
de pallier la gêne respiratoire, qu'éprouvent ces patients, en réalisant une
ablation d'une corde vocale rétablissant ainsi une entrée d'air suffisante.
En cancérologie il convient, comme toujours, de se
montrer très prudent ; le laser CO2 est toutefois indiqué à titre curatif pour
les tumeurs de la glotte. En cas d'envahissement massif du vestibule laryngé,
il permet de réduire le volume tumoral.
- Pathologie
nasale :
L'hypertrophie des cornets du nez, affection peu grave
mais gênant la respiration nasale et favorisant le ronflement, est facilement
corrigée au laser néodyme-YAG (avec fibre optique). Ce dernier s'avère très
efficace, mais surtout très rapide.
- Pathologie
auriculaire :
Le laser a été utilisé dès 1967 dans ce domaine.
Actuellement, c'est le laser à argon, dont le rayonnement est très fortement
absorbé par les pigments sanguins, qui est généralement employé : tous les
tissus mous de l'oreille moyenne peuvent être ainsi réséqués, vaporisés, sans
saignement, ce qui est capital en microchirurgie auriculaire.
En oto‑neuro‑chirurgie, en particulier pour
le traitement des tumeurs nerveuses bénignes du nerf acoustique, l'apport du
laser à CO2 est majeur : il permet d'aborder la lésion sans saignement
important (car il coagule les micro‑vaisseaux), de vaporiser la partie
centrale du neurinome, de séparer progressivement et sans dommage la tumeur des
tissus avoisinants.
f)
Broncho‑pneumologie :
La première intervention sur les bronches au laser a été
réalisée en 1978, par bronchoscopie, à l'aide d'un néodyme-YAG assorti d'une
fibre optique.
Si lors des premiers essais, les lasers à l'argon et au
néodyme-YAG ont été mis en concurrence, l'unanimité s'est rapidement faite sur
la prééminence du second : l'émission du CO2 ne pouvant être, à ce jour,
véhiculée par fibre optique sur une distance suffisante.
Les indications du laser sont pratiquement limitées aux
tumeurs et aux sténoses de la trachée et des bronches.
- Les
endoscopes :
Rappelons que les endoscopes sont des appareils
constitués d'un tuyau nanti d'un système optique permettant de pénétrer,
d'examiner et d'intervenir à l'intérieur d'une cavité naturelle ou d'un organe.
Il existe deux types d'endoscopes (rigide et souple) :
- Les fibroscopes souples, peuvent être aisément
introduits dans l'arbre trachéo‑bronchique jusqu'aux bronches de faible
diamètre, sans anesthésie générale, l'intervention étant absolument indolore.
Cependant il est impossible toutefois, avec ces appareils, de réaliser en même
temps la résection laser et l'aspiration des produits de sécrétion , ce qui
complique l'intervention.
- Les bronchoscopes, rigides, dont l'introduction
délicate nécessite une anesthésie générale parfois bien difficile à réaliser
chez des patients en détresse respiratoire, présentent des avantages non
négligeables : vision élargie du champ opératoire, possibilité de procéder
conjointement à la résection laser et à l'aspiration des sécrétions
hémorragiques et bronchiques, ou d'interrompre le geste chirurgical pour
oxygéner fortement le malade en cas d'asphyxie pendant l'opération.
- Applications :
Les tumeurs bénignes de la trachée et des bronches,
relativement rares, sont peu hémorragiques, de forme généralement sphérique
et/ou pédiculée : réséquables en quelques tirs, elles représentent une
indication parfaite de la laserthérapie.
Les granulomes inflammatoires se développent sur les
cicatrices de trachéo-bronchique. Le laser permet leur destruction sans
atteinte du tissu porteur et évite une évolution fibreuse éventuelle
susceptible d'entraîner un rétrécissement gênant la respiration.
Les cancers à développement intratrachéal ou
intrabronchique entraînent une obstruction des voies respiratoires et une
asphyxie du sujet. Le laser ne peut vaporiser la tumeur jusqu'à “ ses racines »
et ne représente qu'un moyen palliatif d'efficacité temporaire, permettant
toutefois au malade de retrouver un confort respiratoire difficile à procurer
par d'autres méthodes.
Les lésions fibreuses survenant à la suite d'intubation
ou de trachéotomie entraînent un rétrécissement ou sténose trachéo‑bronchique.
Lorsque ces lésions ne représentent qu'un diaphragme fibreux, il est aisé de
les volatiliser au laser, sans hémorragie, et de rétablir le calibre
bronchique.
- Conclusion :
Actuellement les indications de l'utilisation du laser au
néodyme-YAG en broncho‑pneumologie sont parfaitement codifiées. Les
recherches modernes portent sur l'étude de fibres pouvant transporter les
rayonnements infrarouges lointains du laser à CO2 : récemment une fibre
japonaise a permis de le faire sur des distances n'excédant pas 30 centimètres,
ce qui est trop peu, mais constitue un début. Ce rayonnement aurait un intérêt,
sans doute limité mais certain, en pneumologie.
g) Gastro‑entérologie :
Les lasers ne remplacent pas le bistouri en gastro‑entérologie,
mais permettent, grâce à l'endoscopie, de traiter par les voies naturelles,
sans “ ouvrir le ventre », certaines hémorragies, perforations et tumeurs du
tube digestif.
- Hémorragies
digestives :
Ce sont les hémorragies qui ont bénéficié en premier de
la laserthérapie en pathologie digestive.
Le traitement se fait généralement en urgence et consiste
à effectuer une photocoagulation des vaisseaux saignants par voie endoscopique.
Les lasers utilisés sont l'argon ou le YAG. Le premier,
mieux absorbé par les pigments sanguins, nécessite moins d'intensité (en
général d'environ 10 watts), mais pénètre 4 à 5 fois moins profondément que le
second, qui avec une puissance de 60 à 100 watts assure une hémostase de
vaisseaux de plus gros diamètre et plus profondément situés.
Durant l'intervention, l'extrémité de la fibre optique
est maintenue à 1 ou 2 centimètres de la surface saignante. Afin d'éviter les
brûlures trop profondes, causes de perforation et de péritonite, les tirs
doivent être courts : 1,5 seconde en moyenne avec le laser à argon dont le
champ doit être constamment nettoyé par un jet d'air coaxial afin de chasser le
sang (0,2 millimètres de sang suffisent à absorber totalement le rayonnement), et
0,5 à 1 seconde pour le néodyme-YAG dont la cible doit être rincée à l'eau pour
rester visible. Le traitement doit être continué jusqu'à l'arrêt complet de
l'hémorragie.
Le laser à néodyme-YAG, plus efficace mais plus dangereux
que le laser à argon, doit donc être réservé aux hémorragies sévères.
Les hémorroïdes sont généralement gênantes ou
douloureuses et se manifestent souvent par des saignements que l'on peut voir
sur les selles. Elles se soignent médicalement si elles ne sont pas trop
développées, ou s'opèrent classiquement, mais aussi par le froid (elles se “
dessèchent » après cryocoagulation), ou au laser CO2 qui les coagule et les
détruit d'une façon très précise : les suites opératoires sont nettement moins
douloureuses.
- Tumeurs
du tube digestif :
Il s'agit le plus souvent de tumeurs épithéliales,
développées à partir de la couche cellulaire interne du conduit digestif, dont
le type est variable selon les organes.
La photodestruction laser s'inscrit parmi les méthodes de
traitement local d'une tumeur : elle comporte des avantages (simplicité de
l'opération, faible durée de l'immobilisation du patient) et des limites
(impossibilité de détruire complètement une tumeur qui envahit toute
l'épaisseur de la paroi ou la dépasse). Son indication ne peut être portée
qu'après avoir fait une certaine estimation.
Les tumeurs bénignes
peuvent être détruites avec une grande sécurité, sous coloscopie, au
laser à néodyme-YAG à travers une fibre gainée et ventilée. Cette intervention,
qui ne comporte pas d'hospitalisation, semble constituer une bonne prévention
des cancers du côlon et comporte moins de récidives que l’électrocoagulation
classique.
Il y a aussi le traitement des tumeurs malignes qui peut
être à visée curative ou palliative. Le laser utilisé est toujours le
néodyme-YAG à forte puissance, pour ses qualités de pénétration et de
coagulation entraînant la destruction des tissus.
h) Urologie :
En urologie, le laser s'est développé tant pour la
chirurgie à ciel ouvert que pour l'endoscopie. En chirurgie classique, les
lasers à argon, à CO2 et à Nd : YAG apportent leurs qualités respectives, mais
ne sont qu'un supplément.
- Chirurgie
endoscopique :
L'utilisation des lasers en endoscopie nécessite, vu la présence
d'urine, une adaptation du matériel. Il est ainsi possible de traiter certaines
lésions de l'urètre et de la vessie. L'intervention, indolore, ne nécessite ni
anesthésie ni hospitalisation et elle n'est pratiquement pas hémorragique. Les
suites opératoires sont excellentes et les récidives moins fréquentes que par
les méthodes classiques.
- Traitement
des calculs urinaires :
La crise de
colique néphrétique est horriblement douloureuse : elle se traite par des sédatifs. . Pour éviter les récidives, lorsqu'on
a localisé le calcul (concrétion pierreuse), il faut l’éliminer.
On peut, de nos jours, utiliser la lithotriptie laser par
voie endoscopique. Le principe est de créer une onde de choc à l'intérieur même
de la concrétion. Pour ce faire, il est nécessaire d'amener l'énergie au
contact du calcul, repéré par endoscopie des voies urinaires : une fibre
optique fine (de 200 ou 400 microns de diamètre) transmet les impulsions du
laser, très brèves, et concentre une puissance instantanée considérable dans la
cible où l'énergie photonique se transforme en vibrations acoustiques sous
l'impulsion du choc, fragmentant ainsi le calcul en morceaux suffisamment menus
pour être éliminés naturellement par les voies urinaires.
i) Gynécologie :
En gynécologie, le laser permet avant tout de traiter les
affections qui touchent la fonction de reproduction et la pathologie tumorale,
bénigne, précancéreuse ou maligne, affections par les voies naturelles (vulve,
vagin, col et isthme utérins) ou trans‑abdominales (utérus, trompes, bas‑ventre).
Le laser utilisé est principalement le CO2, soit
directement, c'est‑à‑dire à l'aide d'un bras articulé et d'une
pièce à main au cours d'interventions classiques à ciel ouvert, soit couplé à
un endoscope trans‑abdominal (cœlioscope) ou à un appareil de
microchirurgie.
- Pathologie
de la vulve et du col :
Dans les tumeurs de la vulve : la vulvectomie peut se faire au laser à CO2,
à la pièce à main, avec l'avantage sur le bistouri d'une meilleure
cicatrisation et de suites opératoires moins pénibles.
Les dysplasies du col de l'utérus sont caractérisées par
la présence d'un revêtement cellulaire anormal. L’évolution vers la
cancérisation est possible et dans ce cas la vaporisation laser est utilisée.
Cette méthode est facile, ne nécessitant qu'une puissance de 15 à 25 watts,
rapide et sans anesthésie.
Par sa précision de destruction en surface et en
profondeur, le caractère aseptique de l'intervention, la cicatrisation plus
rapide et de meilleure qualité, l'absence de conplication, le laser à CO2
parait nettement supérieur aux autres techniques de traitement local
(électrocoagulation, cryothérapie).
- Tumeurs
de l’ovaire :
Souvent découvertes à un stade tardif, les tumeurs de
l'ovaire ne peuvent pas toujours être extirpées en totalité. Après l'opération,
il persiste fréquemment dans le petit bassin des reliquats tumoraux sur les
organes voisins comme l'intestin grêle, le côlon, la vessie, dont la
destruction par les moyens classiques était difficile : le laser permet de les
vaporiser sans faire courir les risques de nécrose que le bistouri électrique
entraînait, ce qui améliore le pronostic.
§ Pathologie des trompes de fallope :
Les interventions au laser sur les trompes et les organes
situés au niveau du bassin peuvent être réalisées au cours d'opérations
gynécologiques classiques et donne des résultats remarquables.
Le traitement des stérilités d'origine tubaire a été
transformé par la combinaison du microscope opératoire et du laser à CO2, dont
la finesse d'impact a rendu possible la réfection endoscopique très précise et
la reperméabilisation de trompes utérines et de pavillons obstrués, ainsi que
la reconstitution des trompes sectionnées ( la plupart des femmes ainsi
traitées ont pu devenir enceintes et mener à bien leur grossesse).
j) Cardio‑angéiologie :
La pathologie cardio‑vasculaire peut se diviser en
deux parties:
‑ maladies du muscle cardiaque.
‑ maladies des vaisseaux.
Il est certain que les lasers ne peuvent rien pour le
muscle cardiaque, par contre en pathologie artérielle, leur utilisation est
effective, bien que récente. Elles sont surtout utilisées pour désobstuer les
artères.
Les premiers essais de photodésobstruction datent de
1980, et les progrès techniques de ces dernières années ont apporté une
amélioration des conditions opératoires : lasers pulsés qui délivrent une
énergie intense en un temps très court et vaporisent l'obstacle sans diffusion
de chaleur (lasers excimères en particulier ne lésant pas la paroi artérielle),
et surtout, peut‑être, cathéters multifibres. Ces derniers offrent, grâce
à leurs très nombreuses fibres optiques ultrasouples une grande sécurité de
guidage, un accès relativement facile des artères, y compris celles qui
irriguent le cœur (coronaires), et permettent de traverser plus aisément les
rétrécissements sans risque d'entraver la circulation dans l'organe.
Actuellement, ce ne sont plus seulement les grosses artères des jambes qui sont
traités. Cependant, cette méthode reste expérimentale et en phase d'évaluation.
k) Rhumatologie :
L'exploration endoscopique des articulations
(arthroscopie) s'est beaucoup développée depuis une décennie. Le matériel s'est
perfectionné tout en s'affinant en ce qui concerne le diamètre. Elle n'est plus
seulement un procédé d'investigations exceptionnelles, mais un moyen de pratiquer
des interventions à moindres dégâts.
Le laser a pu pénétrer la spécialité et nul doute que les
lasers, à excimères en particulier, devraient être très performants dans cette
spécialité pour découper les ligaments sans les léser, volatiliser des concrétions
cartilagineuses ou fibrosseuses...
m)
Odonto‑stomatologie :
Dès
1963 des études ont été faites, aux USA puis en Allemagne, sur la possibilité
d'application du laser à l'art dentaire. Mais ces travaux n'ont pas eu de suite
immédiate car, si l'élévation thermique obtenue au niveau de la carie aboutit à
une véritable volatilisation du tissu malade, à une stérilisation de la cavité
et à une restructuration superficielle des parois laissant la dent prête à être
obturée, ces avantages étaient entachés d'un inconvénient majeur : la dent
était mortifiée par le traitement photonique! L'analyse a montré que ce sont
les phénomènes mécaniques provoqués par les impulsions répétées des émissions
des lasers à rubis qui entraînent, par effet de choc, la destruction du paquet
vasculo‑nerveux de la pulpe dentaire, et la perte de vitalité de la dent.
Les lasers continus n'ont pas ces inconvénients, et c'est
le développement des lasers à CO2, à néodyme-YAG et à argon qui a permis un
renouveau thérapeutique dans cette discipline.
- Les
caries :
Au niveau de la couronne (recouverte d'émail), la carie
correspond à une destruction localisée de la dent. Elle débute par une atteinte
de l'émail, fissuration ou décalcification, libérant ainsi les constituants
minéraux et favorisant la production de micro‑organismes et de leurs
toxines qui s'accompagnent généralement de douleurs, pour aboutir à la perte de
la vitalité dentaire.
Les industriels ont réalisé pour les dentistes des lasers
à CO2 miniaturisés, émettant en continu, qui peuveut tenir en main comme un
gros crayon, et dont l'extrémité peut être dirigé vers les faces postérieures
des dents. Ils se manipulent comme une fraise dentaire, à la différence que le
praticien n'a plus le contact tactile avec la dent. A une puissance de 4 watts,
ce type de laser provoque, par de rapides balayages de la zone atteinte, une
véritable excision de la carie, par couches de 150 microns (l'abrasage est
beaucoup plus précis qu'avec la fraise qui enlève un millimètre à chaque
passage). De plus la température de la pulpe ne s'élève pas de plus de 2 degrés
pour des impacts de 4 watts ne dépassant pas 0,5 seconde, ce qui permet de
conserver vivantes des dents profondément cariées, alors qu'avec la technique
classique de fraisage il serait absolument nécessaire de procéder à leur
dévitalisation. Ces caractéristiques ont un intérêt thérapeutique majeur dans
la réalisation des coiffages (procédés destinés à isoler la pulpe afin de
maintenir la vitalité dentaire).
- Les
foyers périapicaux (clavité où se trouve la
pulpe) :
Lorsque la dent cariée a été traitée trop tardivement, la
pulpe s'infecte, l'infection fuse jusqu'à la pointe de la racine et peut
déclencher un abcès : il est alors nécessaire de désinfecter l'intérieur de la
dent. Pour ce faire, il faut «dévitaliser» la dent en procédant à l'extraction
de la pulpe, à un nettoyage, à l’élimination de la partie de la racine infectée et au remplissage de la
totalité de la cavité résiduelle avec une pâte désinfectante.
Le laser à CO2 permet, après obturation du canal
radiculaire par la pâte, de stériliser le bout de la racine par irradiation de
toutes ses faces et de son extrémité grâce à un miroir réfléchissant à 90°.
Cette méthode permet d'éviter la résection de la partie infectée de la racine
ce qui est un gros avantage (si la racine est coupée trop court, la dent ne
tient plus!). Elle n'entraîne aucun passage de microbes dans le sang ( la
pointe de la racine est là où pénètrent les éléments vasculaires et nerveux) et donne une certitude de stérilisation du
foyer apical.
§
Laser et chirurgie maxillo-faciale :
La chirurgie des os maxillaires, où sont enchâssées les dents, est faite
avec le laser à CO2, mais d'une puissance de 60 watts comme en ORL. Il
sectionne comme un bistouri, volatilise, stérilise instantanément les tissus,
évite leur saignement, ne provoque qu'un trauma minime, n'entraîne pas de
sensation désagréable ni de contraction musculaire. Il réduit le temps de
cicatrisation et d'hospitalisation et ne nécessite en règle générale, pas de
traitement post‑opératoire.
§
Prospectives :
D'autres types de laser
ont été expérimentés :
- le Néodyme-YAG présente un intérêt dû à son action sélective sur les
tissus colorés : il permettrait l'élimination des caries situées dans les
sillons des dents, ce qui serait très utile, en particulier chez les enfants.
- l'argon n'a aucun effet probant sur l'émail, mais, éliminant le cément
(jointure des dents) infecté au niveau des dents déchaussées.
III Conclusion :
Les lasers sont donc maintenant indispensables dans le
milieu médical car ils permettent de soigner des maladies qui seraient
difficiles à guérir sans ces machines à photons. De plus, leur capacité à
véhiculer sur de longues distances des énergies extrêmement concentrées leur
présage un avenir plus que certains. Les lasers puissants, chirurgicaux en
particulier, sont donc dangereux : ils peuvent brûler les opérés hors de la
zone de visée, ainsi que les opérateurs, et détériorer les objets qu'ils sont
susceptibles de croiser sur leur trajet. Il est donc indispensable d'assurer la
protection:
-
Du personnel travaillant dans la salle d'opération par le port de lunettes
filtrant spécifiquement la longueur d'onde du ou des lasers utilisés.
- Du patient, par des draps et un pansement oculaire
humidifié.
- Des instruments inflammables par un revêtement
métallique.
Il faut, de plus, par une bonne collaboration entre
chirurgien et anesthésiste, veiller à ne pas utiliser, dans le champ opératoire,
des matériaux susceptibles d'être enflammés par l'émission laser ou de
provoquer une explosion (tel qu'un mélange trop riche en oxygène en chirurgie
bronchique).
La fumée provoquée par la volatilisation des tissus peut
opacifier le champ opératoire, surtout en endoscopie, et même asphyxier le
malade en chirurgie laryngée ou bronchique. Elle doit être évacuée : divers
systèmes de ventilation ont dû être adaptés à chaque cas, mais la simple
ventilation de la fibre optique peut parfois suffire.
L’utilisation du laser oblige donc à prendre quelques
dispositions et donc des contraintes mais ces points négatifs ne sont que des
formalités car leur efficacité est telle que l’on ne peut envisager
d’abandonner leur emploi dans le milieu hospitalier.